- 話題
-
GemVaxが、進行性核上性麻痺の第2a相臨床試験のトップライン結果をNeuro2024で発表
- 2024/10/31 15:35 公開 GemVax & KAEL
-

- トップラインは第3相試験への移行を支持し、GV1001を世界初のPSP治療薬として開発する可能性を示している
ソウル(韓国)、2024年10月31日 /PRNewswire/ -- GemVax & KAEL Co., Ltd.(「GemVax」、KOSDAQティッカー:082270)が、進行性核上性麻痺(「PSP」)の治療薬として開発中のペプチド薬GV1001の第2a相臨床試験(「第2a相PSP臨床試験」)のトップライン結果を、カナダのトロントで開催された「Neuro2024:The PSP and CBD International Research Symposium(Neuro2024:PSPおよびCBD国際研究シンポジウム)」で、現地時間10月24日午後4時45分に発表しました。
PSPは、パーキンソン病と同じく歩行障害、早期転倒、垂直眼瞼麻痺、固縮、振戦、認知機能低下などの症状を引き起こす変性疾患ですが、パーキンソン病よりも進行が速く、現在のところ根本的な治療法がありません。PSPは、PSP-リチャードソン症候群(「PSP-RS」)やPSP-パーキンソン症候群(「PSP-P」)など、複数の型に分類されます。PSP-RS型は、それ以外の型のPSPと比較して、タウ・タンパク質の蓄積が多く見られ、小脳、歯状核、橋核、前頭葉、頭頂葉など、より広い領域に影響を及ぼします。
第2a相PSP臨床試験は、韓国の5つのセンターでPSP患者78名を対象に実施されました。24週間、無作為、二重盲検、プラセボ対照、前向き探索的臨床試験です。被験者は、プラセボ、GV1001 0.56 mg、GV1001 1.12 mgのいずれかに1:1:1で無作為に割り当てられました。最初の4週間(1か月間)は週1回、その後は2週間間隔で20週間(5か月間)、合計24週間(6か月間)、薬剤が皮下投与されました。PSP-RS型とPSP-P型の両方の患者が研究に参加する資格がありました。結果は、特にPSP-RS型患者において、低用量群(0.56 mg)でより高い恩恵がありました。
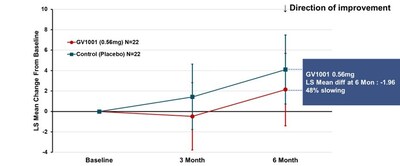
試験の主要評価項目は、GV1001投与24週間後のPSP評価スケールの合計スコア(MMRM法を用いて最小二乗平均で計算)におけるベースライン値からの変化です。これによると、GV1001 0.56 mg投与群では2.14ポイントの悪化となり、プラセボ群の4.10ポイントと比較すると、病気の進行が48%減少したことが示されました(図1参照)。統計的有意性は示されなかったものの、この結果は、現在治療法のない疾患であるPSPの治療薬として、GV1001の潜在的な可能性と、GV1001をさらに臨床試験に進められる可能性を裏付けています。
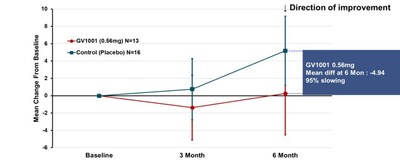
臨床的に典型的なPSPはPSP-RS型と見なされることが多く、この型はPSP患者の大多数を占めています。この型は、他のPSP型と比較して進行が速く、平均生存期間が短くなります。部分集団別解析は、PSP-RS型の患者のみを対象に実施されました。PSP-RS型患者へのGV1001投与24週間後のPSP評価スケール合計スコア平均(単純平均を使用して計算)のベースライン値からの変化は、GV1001 0.56 mg投与群では0.25ポイントの悪化であったのに対し、プラセボ群では5.19ポイントの悪化と4.94 ポイントの差がつきました。つまり、病気の進行が95%減少したことが示されました(図2参照)。
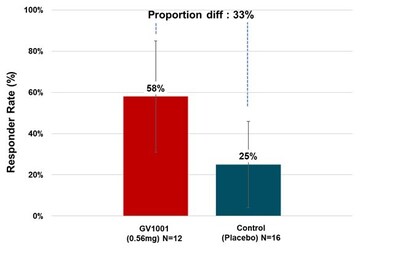
治療群のPSP-RS型患者の多くは、臨床期間中に症状の安定化、あるいは改善を経験しました。ベースライン値と比較して、治療開始から6か月後にPSP評価スケール・スコアが改善または安定した患者の割合に基づくレスポンダー率として計算すると、0.56 mg GV1001群のPSP-RS型患者の58.33%が改善または安定を示したことになります(図3参照)。
第2a相PSP臨床試験におけるGV1001の安全性プロファイルは、これまでの安全性データと一致していました。GV1001の忍容性は概して良好で、薬剤に関連する重篤な有害事象は報告されませんでした。
GemVaxのCSO、Hyungsik Moon(ムン・ヒョンシク)氏は次のように述べています。「この第2a相試験は、最適な投与量を決定し、ペプチドが異なる部分集団にどのように作用するかを調べるための探索的検査です。トップライン結果は統計的に有意ではなかったものの、主試験に進むことを検討できるほどエビデンスは強力であり、GV1001をPSPに対する世界初の治療選択肢として開発する可能性を示しています。」
Neuro2024会議の専門家らは、PSP試験の結果を有望なものとして歓迎し、さらなる進展のために、世界規模でこの薬剤の第3相臨床試験に入ることに大きな期待を表明しました。
「このパイロット試験は、十分なリソースが投入されず、治験期間も6か月と短いものでした。したがって、統計的に有意な確認結果は期待できませんでした」と語るのは、世界的なCRO ICONの医薬品開発担当上級副社長であるPeter Schüler医学博士。「それでも、観察された傾向は、運動能力と認知機能という2つの領域で非常に妥当かつ一貫しており、どちらも低用量グループに恩恵をもたらしています。」
「今回の試験は、第2a相試験の主要目的の1つであった最適投与量を特定し、プラセボ群と比較して病気が完全に安定するという臨床的に意義のある効果を実証しました」とSchüler博士は述べ、「このトップライン結果は、第3相試験に進むための強力な基盤を提供します」と付け加えました。
ミュンヘンのLMU病院神経科長であり、世界的に著名なPSPの専門家であるGünter U. Höglinger博士は、次のようにコメントしています。「新しい作用機序を提示する新薬治験の第2相レベルのデータは、とても興味深いものです。データは予備的なものですが、非常に有望であり、[GV1001]アルツハイマー病の臨床データと一致しています。さらなる進展を期待できますし、[PSP]第3相試験に参加し、試験を主導できることを非常に楽しみにしています。」
CurePSPのディレクターであるKristophe Diaz博士は、「最近行われたGemVaxの臨床試験の結果には勇気づけられました。この結果は、現在治療の選択肢がない患者、その家族、担当医師を含むPSPコミュニティ全体に希望を与えています」と延べ、「この試験を成功裏に終えたことについて、GemVaxにはおめでとうと言いたいです。PSPコミュニティに利益をもたらすさらなる進展を期待しています」と付け加えました。同氏はまた、次のように述べています。「CurePSPは、この悲惨な病気に苦しむ人々に希望と進歩をもたらす取り組みに協力し、その活動の支援に引き続き尽力します。」
PDFをダウンロード:https://mma.prnewswire.com/media/2542940/2024_10_29__GemVax_Announces_Topline_Results.pdf
第2a相PSP臨床試験(NCT05819658)について
第2a相PSP臨床試験は、PSP患者の治療におけるGV1001 0.56 mgまたは1.12 mgの安全性と有効性をプラセボ群と比較して評価するための24週間の多施設共同、無作為、二重盲検、プラセボ対照、前向き第2a相探索的臨床試験です。この検査の主要アウトカムは、GV1001投与24週間後のPSP評価スケールの合計スコアにおけるベースライン値からの変化でした。副次的評価項目には、3か月時点でのPSP評価スケールの合計スコアにおけるベースライン値からの変化、3か月と6か月時点でのMoCA-K、K-FAB、ES-ADLが含まれています。GV1001投与の全体的な安全性も評価されました。
GV1001について
GV1001は、テロメラーゼの主要配列に基づく16個のアミノ酸からなる合成ペプチドです。GV1001は、アルツハイマー病やPSPを含む神経変性疾患の潜在的な治療薬として研究されてきました。神経変性疾患において、GV1001は、グリア細胞の表現型を変え、神経炎症を抑制することが実証されています。PSPの第2a相臨床試験に加え、GV1001のアルツハイマー病の第2相臨床試験が現在、米国と欧州で進められています(NCT05189210)。
PSPについて
進行性核上性麻痺(Progressive Supranuclear Palsy)は、成人期発症の進行性神経変性疾患であり、現在のところ病態修飾薬は存在しません。世界中で約100,000人中7人がPSPに罹患しています。男性により多く見られ、主に60歳以上で発症します。PSPの症状には、バランスの喪失、性格の変化、特に下方向への眼球運動の弱さ、嚥下困難、不明瞭な発語、認知障害などがあります。
GemVax & KAELについて
GemVax & KAEL Co., Ltd.は、韓国に拠点を置く先駆的な臨床段階のバイオ医薬品企業です。進行性核上性麻痺やアルツハイマー病などの神経変性疾患に対する独自の治療薬の開発に取り組んでいます。PSPに関しては、PSP患者におけるGV1001の有効性と安全性を評価するために、GemVaxは現在、第2a相試験を韓国で実施しています。世界規模のPSP臨床試験の準備も進行中です。また、 GemVaxは、アルツハイマー病の第2相臨床試験を米国と欧州で進めています。詳細については、www.gemvax.comにアクセスし、LinkedInをフォローしてください。
将来の見通しに関する記述
このドキュメントには、1995年の米国民間証券訴訟改革法の意味の範囲内で成された「将来予想に関する」記述を含む、またはそれに基づく情報が含まれています。将来の見通しに関する記述には、「計画する」、「するつもり」、「期待する」、「予期する」、「意図する」、「信じる」、「潜在的」、「継続する」および類似の表現などが含まれます。これらの記述では、既知または未知のリスクおよび不確実性の影響を受け、実際の結果が、当該記述で明示または暗示されたものと大幅に異なる可能性があります。既知または未知のリスクおよび不確実性には、以下のものが含まれますが、これらに限定されません:失敗のリスクが高く、十分な有効性、安全性の考慮、またはその他の要因の欠如により、規制当局の承認の前後のどの段階でも失敗が発生する可能性がある前臨床および臨床プログラムの時期と結果を含む医薬品研究開発に固有の課題。当社の創薬プラットフォームを活用および強化する能力。開発活動およびその他の企業目的のための資金を調達する能力。当社の共同活動の成功。医薬品候補の規制当局の承認を取得し、最終的に商品化する能力。知的財産保護を取得、維持、および施行する当社の能力。当社の技術システムに対するサイバー攻撃またはその他の混乱。主要な従業員を引きつけ、やる気にさせ、維持し、当社の成長を管理する能力。インフレおよびその他のマクロ経済的な問題。それ以外のリスクおよび不確実性。あらゆる「将来の見通しに関する記述」は、経営陣の現在の見積もり、予測、および推定に基づくものであり、新たな情報や今後の進展、もしくはその他の要因の結果か否かを問わず、該当法によって義務付けられている場合を除き、GemVaxはそのような記述を修正または更新する義務を負わないものとします。
-
![]()
11/24 13:30 カナロコ by 神奈川新聞 藤沢の市民オペラ「魔笛」、伸びやかな歌声を聴いて 12月公演の出演児童も意気込み「ドイツ語の発...
-
![]()
新着 11/25 19:21 tvkニュース 神奈川県が総額10億円余りの補正予算案などを県議会に提出
-
![]()
11/24 15:50 カナロコ by 神奈川新聞 【DeNA】筒香、知野ら現役選手が指導 キッズフェス、小学生約2千人参加
-
![]()
新着 11/25 12:01 デイリースポーツ 広島商は初出場初優勝ならず 達川光男擁した1973年以来51年ぶりの横浜との対決 終盤驚異の粘...
-
![]()
11/24 18:57 FNNプライムオンライン 全国的に師走並みの寒さに…クリスマスマーケット、伝統の餅つき、“ご当地丼総選挙”など各地でイベント
-
![]()
新着 11/25 12:16 CDジャーナル 横浜流星主演映画『正体』×ヨルシカ、本編映像を使用した「太陽」スペシャルMV公開
-
![]()
新着 11/25 08:22 TABIZINE 「Christmas Market in 横浜赤レンガ倉庫」2024年は過去最大規模&ドリカム...
-
![]()
11/24 19:20 カナロコ by 神奈川新聞 丹沢湖マラソン、ゴールにはイノシシ汁が待っている 1400人エントリー
-
![]()
新着 11/25 19:22 tvkニュース 資産運用で得た利益を寄付 鎌倉市と三井住友信託銀行が協定
-
![]()
11/24 10:04 東スポWEB 街を彩るネオンサイン LEDとは違う“ぬくもり”感じてください 輝きに魅せられた職人の半生
-
![]()
11/24 20:20 カナロコ by 神奈川新聞 鎌倉、スチール製カップで藻場を再生 飲食店で販売、回収し海藻の栄養源に
-
![]()
新着 11/25 05:30 カナロコ by 神奈川新聞 むき出しの赤土地面だった丹沢登山道、20年近くかけて緑再生 成長した草木は今や登山者の体に触れるほど